利用游离脂肪酸(OA&PA)刺激肝细胞以验证KLF14对脂质代谢的作用
本文使用游离脂肪酸(250μmol/L PA、500μmol/L OA、24h)处理小鼠原代肝细胞和小鼠肝细胞系AML-12细胞,检测KLF14和脂质代谢基因的变化。结果标明肝细胞内脂质过度累积会抑制KLF14的表达,加重细胞氧化应激,KLF14可促进肝细胞脂肪酸β氧化,缓解细胞内脂质累积,KLF14靶向PPARα信号通路促进肝细胞内脂肪酸β氧化,从而缓解NASH 肝脏脂质累积。上述实验条件和结果,可能会因加药时的细胞密度、代数、状态或耐药性的不同而有所区别,建议先通过浓度、时间梯度实验,摸索最佳药物作用浓度和最佳作用时间。
利用游离脂肪酸(OA&PA)刺激肝细胞以验证KLF14对脂质代谢的作用
南昌大学/博士论文
1. 前言
非酒精性脂肪性肝病(NAFLD)是世界范围内最常见的慢性肝脏疾病之一,在过去几十年中,其全球患病率约为25%,已成为终末期肝病的第二大病因。而我国在1999至2018年间的总患病率已经达到29.6%,超出全球患病率,这也意味着我国近三分之一的人口将面临脂质代谢异常导致的肝脏损伤。
肝细胞是肝脏主要的功能单位,肝脂肪变性是由流入肝细胞的脂质增多或脂质分解减少引起的,因此肝细胞的脂质代谢在非酒精性脂肪性肝炎(NASH)进展中至关重要。当大量脂肪酸进入肝脏内,肝细胞通过促进甘油三酯的合成和脂滴的储存来应对过量的脂质,从而导致脂质积累和脂肪变性。当甘油三酯合成能力不能代偿肝脏脂肪酸的增加时,过量的脂质就会产生脂毒性。Krüppel样因子14(KLF14)是一个具有锌指结构域且进化高度保守的转录因子,广泛表达于肝脏、肌肉、脂肪等组织,其主要作用是调节哺乳动物的基因转录。目前尚未见KLF14在肝细胞中调控脂质代谢的相关研究。
为探究KLF14在肝细胞中脂质代谢的调节作用及其机制,使用游离脂肪酸(OA&PA)处理小鼠原代肝细胞和小鼠肝细胞系AML-12细胞,检测KLF14和脂质代谢基因的变化。
2.实验材料
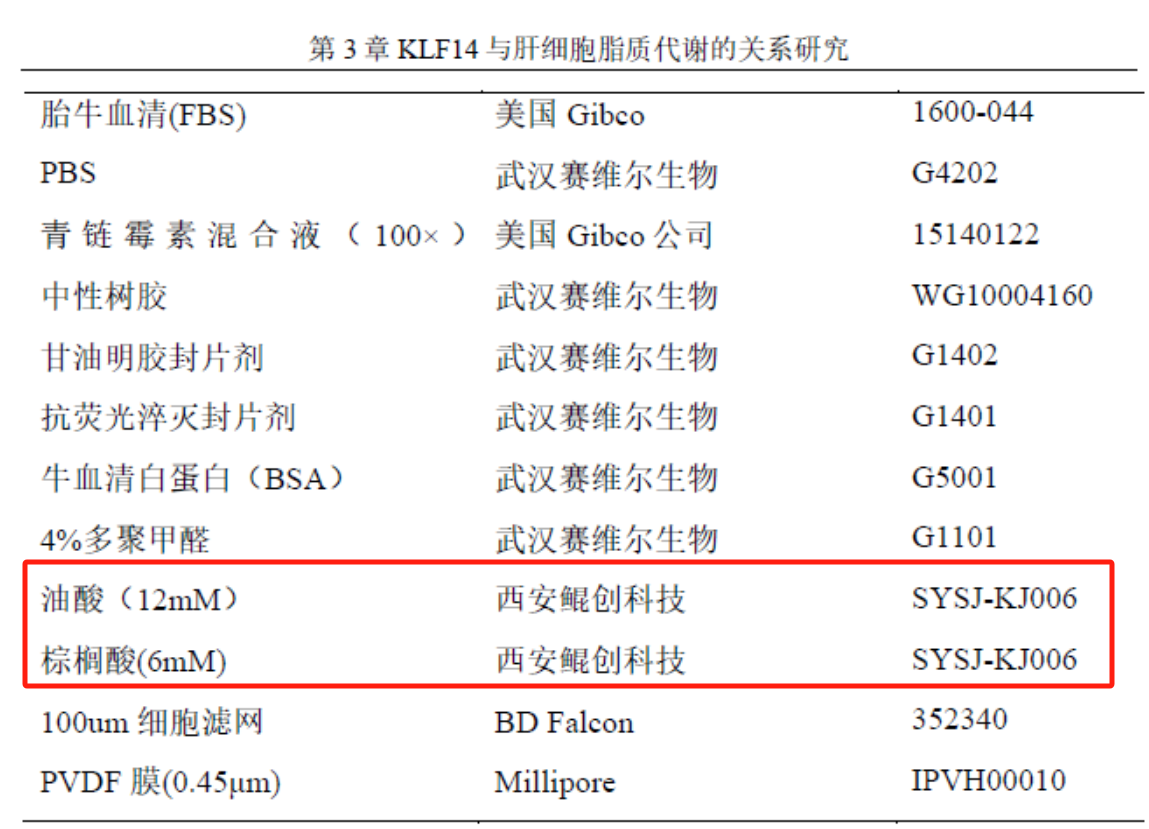
本文采用棕榈酸(钠)和油酸(钠)作为高脂细胞添加剂(原货号SYSJ-KJ006,现货号KC006,Xi'an Kunchuang Technology, China)作为游离脂肪酸(free fatty acids,FFAs)完成体外细胞实验。采用可靠的高脂细胞添加剂,能够保证溶剂无毒、无菌、常温无析出、低温无析出、浓度精准,无需多次加热助溶,显著减少操作步骤,提升实验的稳定性。实际使用时,只需要将高脂细胞添加剂按照比例加入到完全培养基中即可。
3.细胞培养和处理
(1)小鼠原代肝细胞(MPHs)使用含20%FBS的DMEM/F12培养基培养;培养条件:气相,含5%二氧化碳,温度:37摄氏度,培养箱湿度为70%-80%;
(2)AML-12细胞使用含10%FBS的DMEM/F12培养基培养,需添加胰岛素等成分;培养条件:气相,含5%二氧化碳;温度:37摄氏度,培养箱湿度为70%-80%;
(3)游离脂肪酸刺激细胞:使用油酸(oleicacid,OA;12mM)和棕榈酸(palmiticacid,PA;6mM)按浓度比2:1混合作为游离脂肪酸刺激肝细胞,终浓度为750umol/L,刺激24小时;
(4)细胞饥饿实验:MPHs细胞培养贴壁后分为三组,对照组使用含血清的DMEM/F12培养基继续培养,饥饿组更换无血清DMEM/F12培养基培养24小时,恢复血清组使用无血清DMEM/F12培养基培养24小时后,更换有血清培养基培养12小时。
4.部分实验结果
使用游离脂肪酸(油酸和棕榈酸,OA&PA,750umol/L)刺激PMHs和小鼠正常肝细胞系AML-12细胞24小时,并观测肝细胞内ROS水平和KLF14表达的变化。结果显示,游离脂肪酸刺激后,肝细胞内累积大量脂滴,细胞内脂质含量和甘油三酯升高,细胞内ROS水平显著上升,抗氧化基因(SOD2和HO1)受到抑制。无论是在PMHs还是在AML-12细胞中,游离脂肪酸刺激均会导致KLF14表达的下降(图1,图2)。
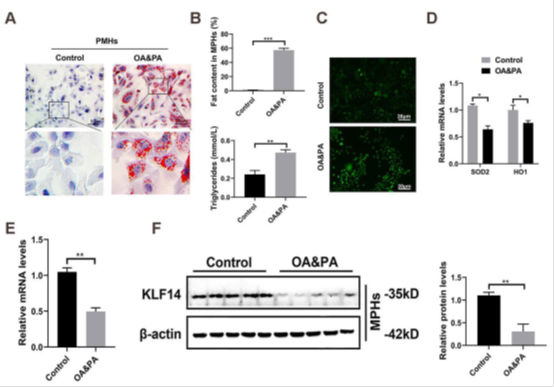
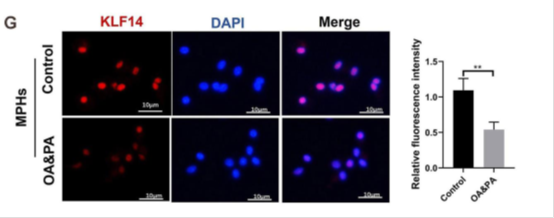
图1 游离脂肪酸(AO&PA)刺激降低PMHs细胞内KLF14表达。A.OA&PA刺激PMHs(OA:PA=2:1)24小时后进行油红染色(200×,放大400×);B.PMHs细胞内脂质含量和TG检测;C.PMHs细胞内ROS水平检测(200×);D.PMHs细胞内抗氧化基因SOD2和HO1表达;E.KLF14在PMHs中的RNA表达;F.KLF14在PMHs中的蛋白表达;G.IF染色检测PMHs中KLF14的表达变化(400×)。*,P<0.05;**,P<0.01;***,P<0.001。
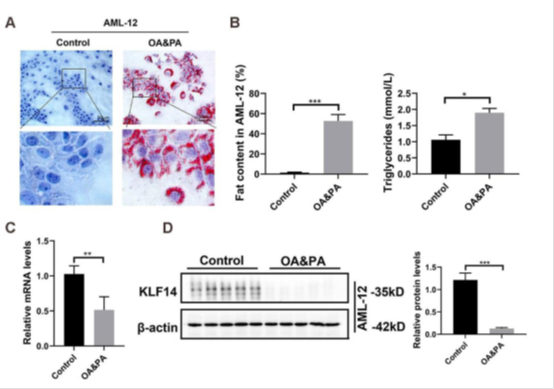
图2游离脂肪酸(AO&PA)刺激降低AML-12细胞内KLF14表达。A.AO&PA刺激AML-12(OA:PA=2:1)24小时后进行油红染色(200×,放大400×);B.AML-12细胞内脂质含量和TG检测;C.KLF14在AML-12中的RNA表达;F.KLF14在AML-12中的蛋白表达。*,P<0.05;**,P<0.01;***,P<0.001。
小编有话说:
本文使用游离脂肪酸(250μmol/L PA、500μmol/L OA、24h)处理小鼠原代肝细胞和小鼠肝细胞系AML-12细胞,检测KLF14和脂质代谢基因的变化。结果标明肝细胞内脂质过度累积会抑制KLF14的表达,加重细胞氧化应激,KLF14可促进肝细胞脂肪酸β氧化,缓解细胞内脂质累积,KLF14靶向PPARα信号通路促进肝细胞内脂肪酸β氧化,从而缓解NASH 肝脏脂质累积。上述实验条件和结果,可能会因加药时的细胞密度、代数、状态或耐药性的不同而有所区别,建议先通过浓度、时间梯度实验,摸索最佳药物作用浓度和最佳作用时间。
参考文献
陈晓燕. KLF14在非酒精性脂肪性肝炎中调控肝细胞脂质代谢的作用及其机制研究[D],博士论文,2024(5).



